細(xì)胞治療時(shí)代,全球臨床批準(zhǔn)的細(xì)胞產(chǎn)品大全
2023-06-15 11:09:15 來源:
細(xì)胞療法,是指把活細(xì)胞送到患者體內(nèi),調(diào)節(jié)、替換或清除異常細(xì)胞,從而實(shí)現(xiàn)再生修復(fù)或免疫治療的過程。
下文,我們將分別介紹已經(jīng)獲得各國(guó)監(jiān)管機(jī)構(gòu)批準(zhǔn)上市的細(xì)胞治療產(chǎn)品。
1、全球臨床批準(zhǔn)的細(xì)胞產(chǎn)品
免疫細(xì)胞,目前只有T細(xì)胞和DC產(chǎn)品被批準(zhǔn)上市。其中大多數(shù) T 細(xì)胞產(chǎn)品是用于血液系統(tǒng)惡性腫瘤的CAR-T療法,而 DC 產(chǎn)品是用于治療實(shí)體腫瘤的疫苗。
臨床批準(zhǔn)的免疫細(xì)胞產(chǎn)品
目前,全球范圍內(nèi)共批準(zhǔn)了9種T細(xì)胞相關(guān)產(chǎn)品,其中美國(guó)FDA批準(zhǔn)上市6 款CAR-T 產(chǎn)品,中國(guó)NMPA批準(zhǔn)上市2款CAR-T產(chǎn)品。有意思的是,韓國(guó)KFDA批準(zhǔn)上市1款CIK產(chǎn)品。

各國(guó)獲批免疫細(xì)胞( T 細(xì)胞)一覽
CAR的兩個(gè)基本部分包括用于識(shí)別癌細(xì)胞表面抗原的細(xì)胞外靶點(diǎn)結(jié)合域和細(xì)胞內(nèi)信號(hào)部分,由共同刺激和激活域組成,啟動(dòng)包括激活、擴(kuò)增和細(xì)胞殺傷在內(nèi)的過程。值得注意的是,所有經(jīng)批準(zhǔn)的CAR-T產(chǎn)品都是自體的,并且含有靶向CD19的CAR(CD19是B細(xì)胞表面標(biāo)記物)。1. CAR-T細(xì)胞療法
目前全球市場(chǎng)上共有8種CAR-T產(chǎn)品獲上市批準(zhǔn)。2017年,美國(guó)FDA批準(zhǔn)全球第一款CAR-T細(xì)胞療法Kymriah。Kymriah適用于復(fù)發(fā)性、難治型以及青少年B細(xì)胞急性淋巴性白血病(ALL) ,主要用于青少年、兒童患者。
2020年,第三款CAR-T產(chǎn)品Tecartus獲得美國(guó)FDA批準(zhǔn)。Tecartus適用于治療成人r/r套細(xì)胞淋巴瘤(MCL),這是一種侵襲性、罕見的非霍奇金淋巴瘤。Tecartus制備過程包括一個(gè)豐富T細(xì)胞群的步驟,并從患者外周血單個(gè)核細(xì)胞(PBMC)中去除循環(huán)腫瘤細(xì)胞(CTC)。目的是防止CAR-T細(xì)胞在體外制備過程中活化和隨后耗盡。
2. CIK細(xì)胞療法
目前全球市場(chǎng)上只有1種CIK產(chǎn)品獲上市批準(zhǔn)。ImmunCell-LC是一種自體細(xì)胞因子誘導(dǎo)殺傷 (CIK)細(xì)胞療法,在2007 年獲得韓國(guó)KFDA 批準(zhǔn),并在2018年獲得美國(guó)FDA孤兒藥稱號(hào)。它被用作肝細(xì)胞癌、腦腫瘤和胰腺癌切除后的輔助治療,通過清除殘余腫瘤細(xì)胞實(shí)現(xiàn)治療。ImmunCell-LC的制備,通過分離外周血單個(gè)核細(xì)胞(PBMC),然后用IL-2和抗CD3抗體一起刺激培養(yǎng),最后得到活化的混合的一群異質(zhì)性T細(xì)胞。
3. DC細(xì)胞
目前全球市場(chǎng)上共有3種DC產(chǎn)品獲上市批準(zhǔn)。DC 疫苗是免疫細(xì)胞治療另一個(gè)活躍領(lǐng)域,主要采用自體細(xì)胞。

2010年,Provenge獲得美國(guó)FDA批準(zhǔn),用于治療激素難治性前列腺癌。Provenge是美國(guó)FDA批準(zhǔn)的第一個(gè)DC療法,也是FDA批準(zhǔn)的唯一的DC療法。
Provenge制備:收集患者的外周血單個(gè)核細(xì)胞(PBMC),然后用前列腺特異性癌相關(guān)抗原(PAP)和GM-CSF進(jìn)行體外擴(kuò)增獲得。
Provenge療程:
Provenge是由DC為主的多細(xì)胞懸浮液,分3次靜脈注射,每次間隔2周。
Provenge作用機(jī)制:
作用機(jī)制是DC介導(dǎo)的PAP向患者T細(xì)胞呈遞,引發(fā)針對(duì)前列腺癌細(xì)胞的適應(yīng)性免疫反應(yīng)。
2007年,自體DC療法CreaVax被韓國(guó)KFDA批準(zhǔn),用于腎細(xì)胞癌的治療。2017年,自體DC療法APCeden被印度CDSCO批準(zhǔn),用于治療前列腺癌、卵巢癌、結(jié)直腸癌和非小細(xì)胞肺癌等疾病的治療。
臨床批準(zhǔn)的干細(xì)胞產(chǎn)品
截至目前,全球共有21種干細(xì)胞產(chǎn)品已在全球獲得批準(zhǔn),其中12種獲得美國(guó)FDA或歐洲EMA的批準(zhǔn)。其余9種產(chǎn)品主要在亞洲獲得批準(zhǔn)。值得注意的是,獲批產(chǎn)品主要是由造血干細(xì)胞或間充質(zhì)干細(xì)胞組成。另外,還有一個(gè)角膜緣干細(xì)胞產(chǎn)品。
1. 造血干細(xì)胞(HSC)
目前全球批準(zhǔn)的造血干細(xì)胞療法共有 10 種。其中美國(guó)FDA批準(zhǔn) 8 種臍血產(chǎn)品,均用于造血干細(xì)胞移植的治療。歐盟EMA 批準(zhǔn) 2 種基于自體造血干細(xì)胞的基因療法,Strimvelis 用于腺苷脫氨酶缺乏癥(ADA-SCID),Zynteglo 用于治療輸血依賴性地中海貧血癥。
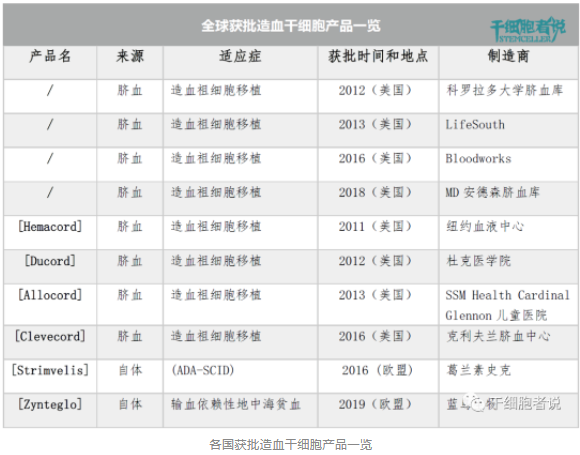
臍血造血干細(xì)胞比其他來源(如骨髓,外周血)的異體造血干細(xì)胞更有優(yōu)勢(shì)。因?yàn)槟氀@得更容易,對(duì)人類白細(xì)胞抗原(HLA)的耐受性更高錯(cuò)配,GVHD的風(fēng)險(xiǎn)較低。
此外,Strimvelis和Zynteglo均是EMA批準(zhǔn)的基于自體造血干細(xì)胞的基因療法。
2016年,EMA批準(zhǔn)Strimveli,適用于腺苷脫氨酶缺乏癥(ADA-SCID),一種由腺苷脫氨酶(ADA)基因編碼突變引起的免疫缺陷疾病。
2019年,EMA批準(zhǔn)Zyntegl, 適用于治療輸血依賴性地中海貧血,這是一種由β-珠蛋白基因突變引起的遺傳性疾病,導(dǎo)致成人血紅蛋白顯著減少或缺失。
2. 間充質(zhì)干細(xì)胞(MSCs)
目前全球批準(zhǔn)的間充質(zhì)干細(xì)胞產(chǎn)品共有 10 種,但沒有一款獲得美國(guó)FDA 的批準(zhǔn)。根據(jù)作用機(jī)制和批準(zhǔn)的適應(yīng)癥,MSCs產(chǎn)品可分為兩大類:組織修復(fù)和免疫調(diào)節(jié)。
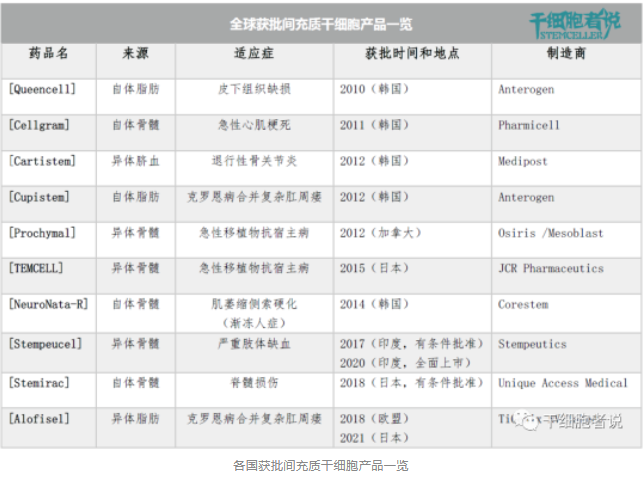
2011年,韓國(guó)KFDA批準(zhǔn)基于MSCs的組織修復(fù)產(chǎn)品Cellgram, 適用于治療急性心肌梗死。
2012年,韓國(guó)KFDA批準(zhǔn)另一種基于MSCs的組織修復(fù)產(chǎn)品Cartistem,適用于重復(fù)性和/或創(chuàng)傷性軟骨退行性病變,包括退行性骨關(guān)節(jié)炎。
2010年,韓國(guó)KFDA批準(zhǔn)一種自體脂肪來源的細(xì)胞產(chǎn)品Queencell,適用于皮下組織缺損的治療。不過,Queencell并非由單一MSCs組成,而是由MSCs、周細(xì)胞、肥大細(xì)胞、成纖維細(xì)胞和內(nèi)皮祖細(xì)胞的混合細(xì)胞組成,類似于SVF。
MSCs具有免疫調(diào)節(jié)功能,可用于調(diào)節(jié)多種疾病的免疫反應(yīng)。其中,七種MSCs產(chǎn)品已被批準(zhǔn),適應(yīng)癥包括克羅恩病(Alofisel、Cupistem)、急性移植物抗宿主病(Prochymal、TEMCELL)、肌萎縮側(cè)索硬化(NeuroNata-R)、脊髓損傷(Stemirac)和Buerger病引起的嚴(yán)重肢體缺血(Stempeucel)。
Alofisel,一種異體脂肪來源MSCs產(chǎn)品。EMA批準(zhǔn)的唯一MSCs產(chǎn)品,適應(yīng)癥是克羅恩病復(fù)雜肛周瘺。作用機(jī)制主要是MSCs抑制活化淋巴細(xì)胞增殖從而減少促炎細(xì)胞因子產(chǎn)生。
Cupistem,一種自體脂肪來源MSCs產(chǎn)品。2012年獲得韓國(guó)KFDA批準(zhǔn),適應(yīng)癥是克羅恩病復(fù)雜肛周瘺。
Prochymal,一種異體骨髓來源MSCs產(chǎn)品。2012年獲得加拿大CFIA批準(zhǔn),適應(yīng)癥是兒童類固醇難治性急性GVHD。
值得注意的是,在3期臨床試驗(yàn)中,Prochymal在SR-aGvHD兒童患者首次類固醇治療失敗后使用,顯示了作為一線治療的安全性、耐受性和有效性。然而,F(xiàn)DA拒絕批準(zhǔn),F(xiàn)DA給出的理由是試驗(yàn)數(shù)據(jù)來自單臂試驗(yàn)而不是隨機(jī)試驗(yàn),建議至少再做一次隨機(jī)試驗(yàn)的數(shù)據(jù)。
其中一些MSCs產(chǎn)品(例如Cellgram, Cartistem、Prochymal)正在當(dāng)前臨床試驗(yàn)中評(píng)估其他適應(yīng)癥,包括酒精性肝硬化、COVID-19引起的急性呼吸窘迫綜合征(ARDS)和軟骨損傷。
除了已經(jīng)批準(zhǔn)的造血干細(xì)胞和MSCs產(chǎn)品外,還有1款角膜緣干細(xì)胞(LSC)產(chǎn)品也獲批。2015年,歐盟EMA批準(zhǔn)Holoclar,用于治療眼部燒傷引起的角膜干細(xì)胞缺乏癥。但是,由于Holoclar以角膜片而非單細(xì)胞懸浮液的給藥方式,我們暫時(shí)不討論。
1. 紅細(xì)胞和血小板
血液制品在治療血液疾病和缺陷方面有著悠久的歷史,但目前并沒有針對(duì)紅細(xì)胞和血小板的特定經(jīng)批準(zhǔn)的產(chǎn)品。
紅細(xì)胞療法適用于治療因血液疾病(即地中海貧血、鐮狀細(xì)胞病、鐵或其他維生素缺乏、再生障礙性貧血)而引起的貧血癥。靜脈注射前,血液必須進(jìn)行ABO血型和RhD匹配。最常用的是紅細(xì)胞輸注,但也可以輸注全血。
血小板輸注用于治療血栓血細(xì)胞減少癥(疾病或癌癥治療引起)。血小板的最佳儲(chǔ)存條件和給藥方案是目前研究的方向。
2. 微生物療法
目前,國(guó)際上并沒有批準(zhǔn)任何一種臨床使用的微生物藥物,但臨床上使用相關(guān)的療法。第一種是糞便菌群移植(FMT),其中健康捐贈(zèng)者的糞便溶液被供應(yīng)到患者的腸道,以改變腸道微生物組組成。雖然可用于臨床治療,但并沒有作為藥品開發(fā)的。第二種是益生菌,包括在非處方藥中廣泛使用的活菌群,也可由臨床醫(yī)生處方。通常被歸類為食品、功能性食品或補(bǔ)充劑,因此也不作為藥物監(jiān)管處理。
小結(jié)與問題
總體來看,干細(xì)胞治療正如雨后春筍般興起,為諸多難治性疾病提供了一條有效治療途徑。從早期對(duì)細(xì)胞療法的質(zhì)疑,到現(xiàn)在似乎又重新變成一個(gè)充滿活力的新興行業(yè)。
目前,中國(guó)對(duì)細(xì)胞治療分別按藥品注冊(cè)和醫(yī)療技術(shù)進(jìn)行“類雙軌制”監(jiān)管。按藥品注冊(cè)開展臨床試驗(yàn),由國(guó)家藥品監(jiān)督管理局(NMPA)監(jiān)管,最終可上市銷售;按醫(yī)療技術(shù)開展臨床研究,由衛(wèi)健委監(jiān)管,最終經(jīng)備案通過后進(jìn)行臨床研究獲得試驗(yàn)數(shù)據(jù),但目前尚未有明確的臨床轉(zhuǎn)化途徑(即收費(fèi))。
Wang LL, Anselmo AC, Mitragotri S, etc. Cell therapies in the clinic. Bioeng Transl Med. 2021
文章圖片均來源于網(wǎng)絡(luò),侵刪!
免責(zé)聲明:本文僅作知識(shí)交流與分享及科普目的,不涉及商業(yè)宣傳,不作為相關(guān)醫(yī)療指導(dǎo)或用藥建議。
文章來源于干細(xì)胞者說,https://mp.weixin.qq.com/s/djNifImvLXbSQ98ItcfhZA

 免費(fèi)服務(wù)熱線:400-6038-558
免費(fèi)服務(wù)熱線:400-6038-558




 贊(
贊( 收藏
收藏
 400-6038-558
400-6038-558





